„Anoda“ a „katoda“ jsou základní pojmy používané v elektrochemii a elektronických obvodech. Tyto dva typy elektrod hrají důležitou roli v různých systémech, od jednoduchých baterií až po pokročilé technologie.
Prozkoumejme jejich rozdíly, pozitivní a negativní označení a jak snadno poznáte, která z nich je negativní nebo pozitivní.
Table of Contents
Co je to elektroda?
Je důležité, abyste pochopili obecnou představu o tom, co elektroda skutečně je, než se pustíte do spletitosti toho, co je katoda nebo anoda. V nejzákladnějším smyslu je elektroda materiál, který napomáhá vedení elektřiny a umožňuje elektrickému proudu vstupovat nebo vystupovat z nekovového média, jako je elektrolytický článek.
Jednoduše řečeno, elektroda slouží jako vodič k vytvoření elektrického kontaktu s nekovovou součástí obvodu.
Co je to anoda?

Polarita elektrody, ať už je to anoda nebo katoda, závisí na typu obvodu. Anoda je elektroda, kde dochází k oxidaci, která vede ke ztrátě elektronů. Když se podíváme na to, co se děje v galvanickém článku (který přeměňuje chemickou energii na elektrickou, jako je vybíjení baterie), anoda funguje jako záporná elektroda, protože během oxidace zůstávají elektrony na elektrodě a proudí vnějším obvodem.
Naopak při elektrolýze, kde elektrický proud pohání tok elektronů v opačném směru, se anoda stává kladnou elektrodou.
Co je katoda?
 Kredit obrázku: Raspberry Pi
Kredit obrázku: Raspberry Pi
Katoda slouží jako místo, kde dochází k redukci, což usnadňuje zisk elektronů. V galvanickém článku se chová jako kladná elektroda, protože ionty podléhají redukci získáváním elektronů z elektrody a následně plátováním.
Na druhou stranu, při elektrolýze je katoda záporným terminálem, přitahuje kladné ionty z roztoku.
Anoda vs. katoda: Vyjasnění polarity
Zpočátku se věřilo, že elektřina proudí z pozitivního do negativního, což je opak toho, co nyní chápeme jako pravdu. Tato raná mylná představa vedla některé k tomu, aby spojovali anodu s negativitou a katodu s pozitivitou.
Nicméně, se správným pochopením role oxidace a redukce v každé elektrodě, bude snadné identifikovat, která z nich je anoda nebo katoda – to závisí na typu obvodu.
Co je elektrolyt v baterii?
 Obrazový kredit: Tinux/gringer/Wikimedia Commons
Obrazový kredit: Tinux/gringer/Wikimedia Commons
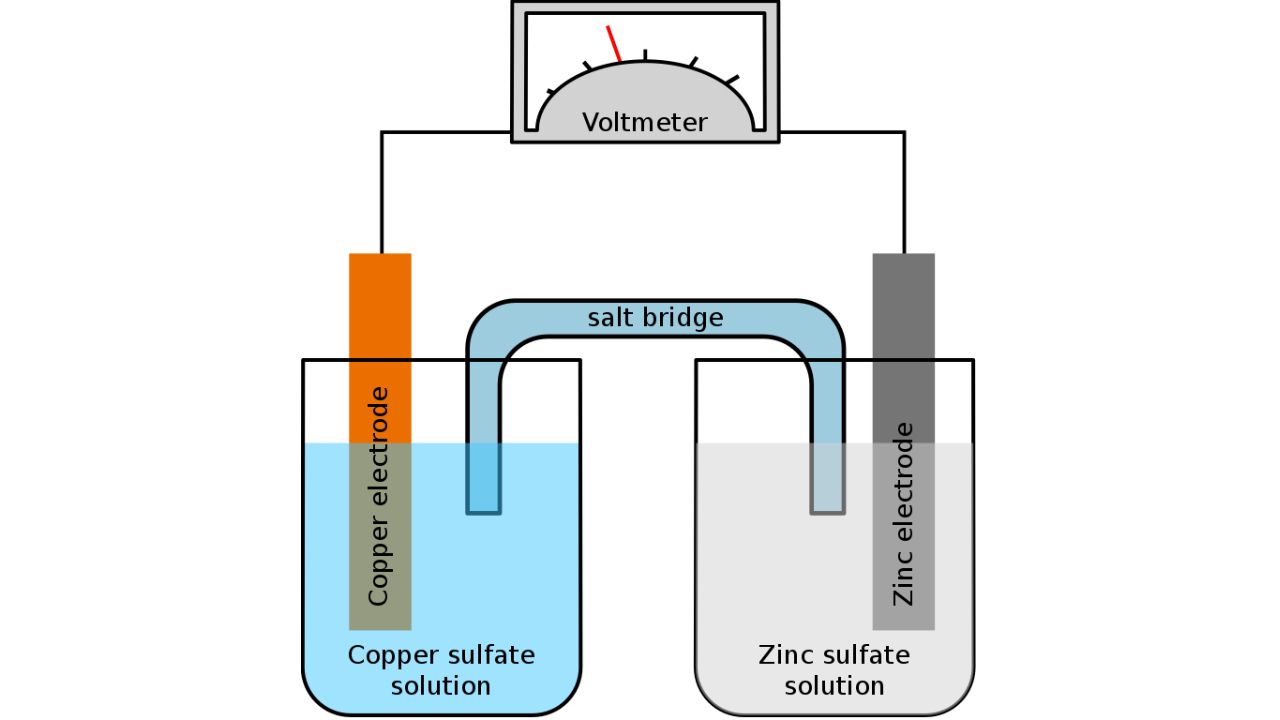
V bateriích se elektrolytem rozumí médium, které umožňuje tok iontů mezi anodou a katodou, přičemž je udržuje elektricky neutrální. Tento pohyb iontů je nezbytný pro chemické reakce, ke kterým dochází během procesů nabíjení a vybíjení. Chcete-li se o tom dozvědět více, přečtěte si, jak fungují lithium-iontové baterie EV.
Který z nich je pozitivní?
Abychom porozuměli polaritám, když mluvíme o elektrodách v článku nebo okruhu, je důležité vzít v úvahu dvě reakce, které probíhají na těchto dvou místech. V galvanickém článku anoda prochází oxidací a funguje jako záporná elektroda, zatímco při elektrolýze se stává kladnou elektrodou. Naopak katoda usnadňuje redukci a slouží jako kladná elektroda v galvanickém článku, ale působí jako záporný terminál při elektrolýze.

